发布时间:2025.07.10 00:00:00
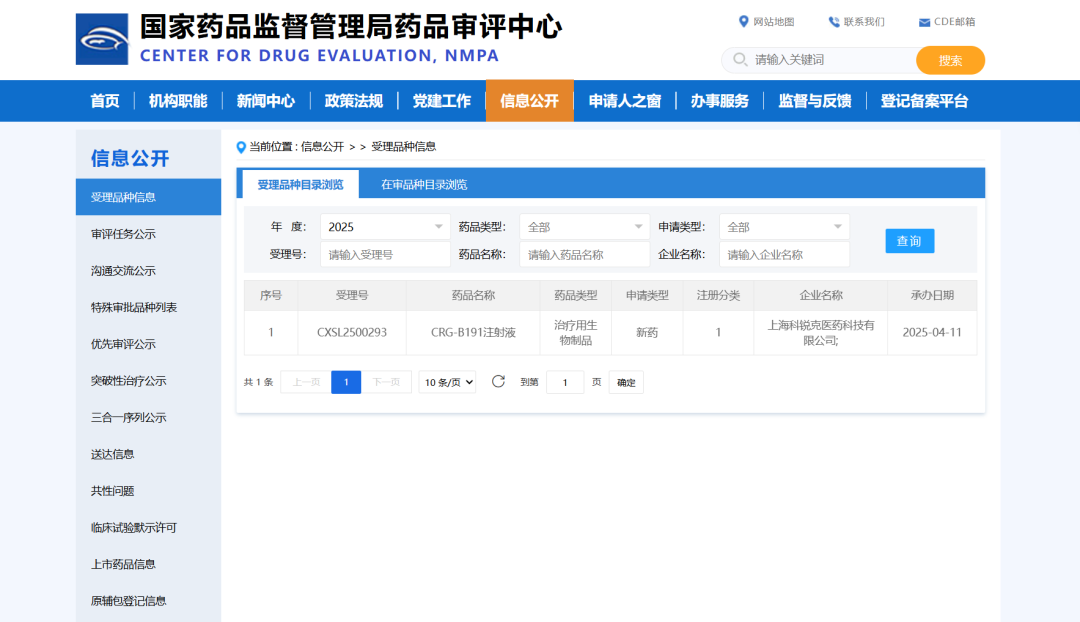
近日,国家药品监督管理局药品审评中心官网显示,上海科锐克医药科技有限公司的 CRG-B191 注射液临床试验申请获得批准。该产品是首个采用 “新一代共价封闭端 DNA 基因组构型” 的 AAV(cceAAV)基因治疗药物,用于治疗湿性(新生血管性)年龄相关性黄斑变性(nAMD)。 关于 CRG-B191 注射液 CRG-B191 注射液采用的 cceAAV 载体具有独特的共价封闭端结构域,具备病毒包装效率高、杂质少、基因组完整性好和外转基因表达效率高等特点,能实现更安全、高效的目的基因递送。经视网膜下注射后,可在视网膜细胞中稳定、持续、高效表达具有自主知识产权的经氨基酸序列优化的抗 VEGF 蛋白,有望实现一次注射长期有效,解决传统治疗中反复眼内注射带来的风险及患者依从性差等问题。 华西海圻的支持 作为国内一流的眼科药物非临床研究评价专业化机构,华西海圻眼科团队在 CRG-B191非临床研究阶段,凭借专业的团队和先进的技术平台,完成了药效学、药代动力学和全面的毒理学评价,保障药物的安全性数据可靠,为该药物的临床试验申请提供了有力支持。 华西海圻始终致力于为创新药物研发提供高质量的非临床研究评价服务,助力更多新药早日进入临床,造福患者。


非临床评价业务联系:028-60662528
电子邮箱:service@glpcd.com
天府新药研究中心:028-60662518-880(前台)
国家成都新药安全性评价中心: 028-85154334-800(前台)


天府新药研究中心:028-60662518-880(前台)
国家成都新药安全性评价中心:028-85154334-800(前台)
电子邮箱:service@glpcd.com
周一至周五 9:00-17:30
咨询热线


隐私条款法律声明网站地图成都华西海圻医药科技有限公司 © 版权所有 蜀ICP备11014334号-1 川公网安备51019002003861号